Приготування розчинів
2. Розрахунки при виготовлені розчинів
Приблизні розчини. При приготуванні приблизних розчинів кількості речовин, які повинні бути взяті для цього, обчислюють з невеликою точністю. Відносні атомні маси елементів для спрощення розрахунків допускається брати округленими іноді до цілих одиниць. Так, для грубого підрахунку відносну атомну масу Феруму можна прийняти рівною 56 замість точного -55,847; для Сульфуру - 32 замість точного 32,064 і т. д.
Речовини для приготування приблизних розчинів зважують на технохімічних або технічних вагах.
Принципово розрахунки при приготуванні розчинів абсолютно однакові для всіх речовин.
Кількість розчину, що виготовляється, виражають або в одиницях маси (г, кг), або в одиницях об'єму (мл, л), причому для кожного з цих випадків обчислення кількості розчинюваної речовини проводять по-різному.
Приклад. Нехай потрібно приготувати 1,5 кг 15%-ного розчину натрій хлориду; попередньо обчислюємо необхідну кількість солі. Розрахунок проводиться згідно пропорції:
| 100 — 15 1500 — x |
x = | 15 · 1500 | = 225 (г) | |
| 100 |
тобто якщо в 100 г розчину міститься 15 г солі (15%), то скільки її потрібно для приготування 1500 г розчину?
Розрахунок показує, що потрібно відважити 225 г солі, тоді води потрібно взяти 1500 - 225 = 1275 (г).
Якщо ж задано отримати 1,5 л того ж розчину, то в цьому випадку за довідником дізнаються його густину, множать останню на заданий об'єм і таким чином знаходять масу необхідної кількості розчину. Так, густина 15 %-нoro розчину натрій хлориду при 15 °C дорівнює 1,184 г/см3. Отже, 1500 мл становить
| 1500 · 1,184 = 1776 (г) | ||||
| 100 — 15 1776 — x |
x = | 15 · 1776 | = 266,4 (г) | |
| 100 | ||||
Точні розчини. При приготуванні точних розчинів обчислення кількостей потрібних речовин перевірять вже з достатнім ступенем точності. Відносні атомні маси елементів беруть по таблиці, в якій наведено їх точні значення. При додаванні (або відніманні) користуються точним значенням доданка з найменшим числом десяткових знаків. Інші складові округлюють, залишаючи після коми одним знаком більше, ніж у доданку з найменшим числом знаків. В результаті залишають стільки цифр після коми, скільки їх є в доданку з найменшим числом десяткових знаків; при цьому здійснюють необхідне округлення. Всі розрахунки проводять, застосовуючи логарифми, п'ятизначні або чотиризначні. Обчислені кількості речовини відважують тільки на аналітичних вагах.
Зважування проводять або на годинниковому склі, або в біксі. Відважену речовину висипають в чисто вимиту мірну колбу через чисту суху лійку невеликими порціями. Потім з промивалки кілька разів невеликими порціями води обмивають над лійкою бнже або годинне скло, в якому проводилося зважування. Лійку також кілька разів обмивають з промивалки дистильованою водою.
Для пересипання твердих кристалів або порошків в мірну колбу дуже зручно користуватися лійкою, зображеної на рис. 1. Такі лійки виготовляють ємністю 3, 6, і 10 см3. Зважувати наважку можна безпосередньо в цих лійках (негігроскопічні матеріали), попередньо визначивши їх масу. Наважка з лійки дуже легко переноситься в мірну колбу. Коли наважка пересипається, лійку, не виймаючи з шийки колби, добре обмивають дистильованою водою з промивалки.
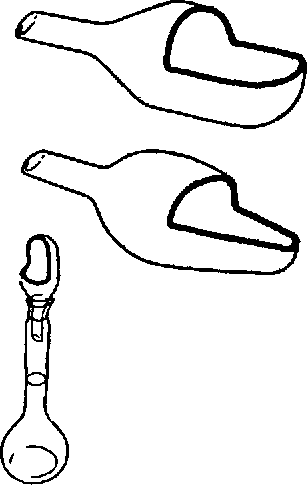
Рис. 1. Лійки для пересипання наважки в колбу.
Як правило, при приготуванні точних розчинів і перенесені речовини в мірну колбу розчинник (наприклад, вода) повинен займати не більше половини ємності колби. Закривши пробкою мірну колбу, струшують її до повного розчинення твердої речовини. Після цього отриманий розчин доповнюють водою до мітки і ретельно перемішують.
Розділи:
© Сущик М. М.